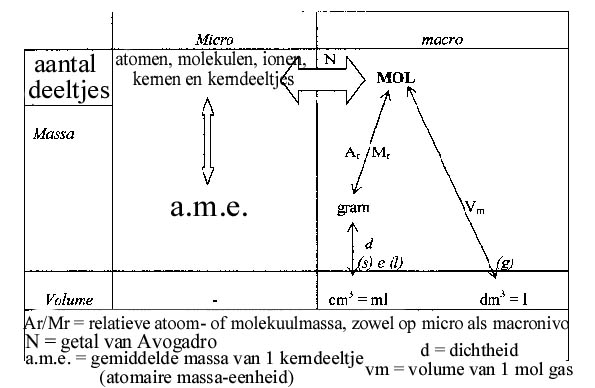
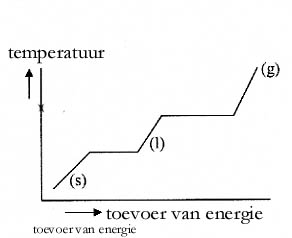
(s) |
(l) |
(g) |
|
(s) |
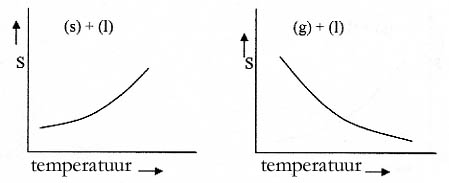
(s) + (s) | (s) + (l) | (s) + (g) |
(l) |
(l) + (s) | (l) + (l) | (l) + (g) |
(g) |
(g) + (s) | (g) + (l) | (g) + (g) |

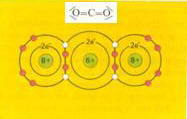
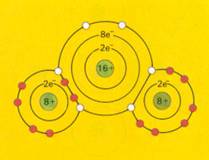
| methaan | ammoniak | water |
| CH4 | NH3 | H2O |
| tetraëder geen dipool |
dipool | dipool |
| k.p. 112 K | k.p. 240 K | k.p. 373 K |
| symmetrisch | asymmetrisch |
 |
 |
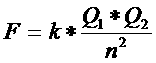
| bindingsafstand | dipoolmoment | |
| HF | 90 x10-12m | 6,4 |
| HCl | 130 x10-12m | 3,5 |
| HBr | 140 x10-12m | 2,7 |
| HI | 160 x10-12m | 1,4 |
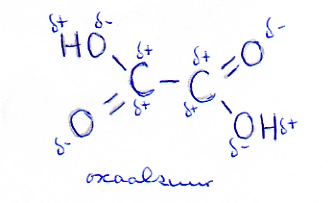
Naast amorfe koolstof zijn er twee bekende roosterstructuren voor koolstof:
Je kunt zo kunstmatig diamant maken uit grafiet. |
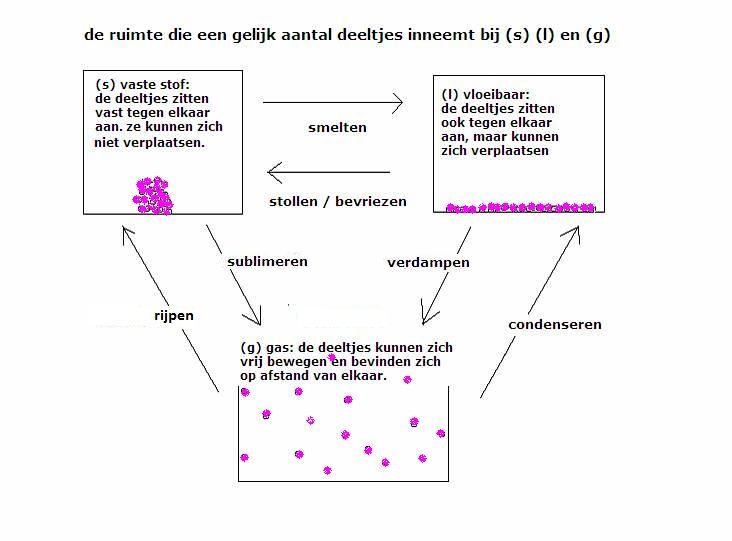
(s)  (l) (l) |
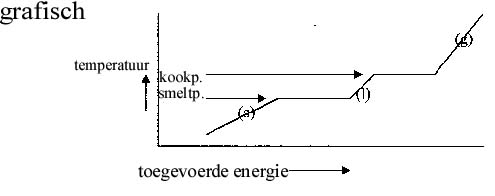
smelten of stollen |
(l)  (s) (s) |
stollen |
(l)  (g) (g) |
koken / verdampen |
(g)  (l) (l) |
condenseren |
(l)  (g) (g) |
verdampen |
(s)  (g) (g) |
sublimeren |
(g)  (s) (s) |
desublimeren of rijpen |
| 1. Het ROOSTER is de belangrijkste factor bij het vaststellen van een smeltpunt
Hoe sterk is het rooster? Hoe gemakkelijk kun je het smelten? Smelten betekent dat het rooster wordt vernietigd en het kost nogal wat energie om een sterk rooster kapot te maken. De sterkte van een ionrooster hangt af van de ladingen van de ionen en van hun onderlinge afstanden. Het rooster van CaO (met ladingen 2+ en 2-) zal moeilijker smelten dan dat van NaCl (met ladingen 1+ en 1-). Behalve de ladingen zijn ook nog eens de ionen van CaO kleiner. Kleinere ionen veroorzaken sterkere roosters. (ze zitten dichter op elkaar) Zouten zullen over het algemeen hoge smeltpunten hebben. Ook de metaalroosters hangen af van ladingen en afstanden. Tussen de metalen bestaan nogal wat verschillen: over het algemeen zal een metaalrooster sterk zijn (dus hoog smeltpunt), maar er zijn uitzonderingen: Kwik(l) is bij gewone temperatuur al vloeibaar. Lood, tin, lithium, natrium, kalium hebben geen sterke roosters. Ze smelten gemakkelijk. Extreem sterk zijn de roosters van: Chroom, Wolffraam en Vanadium. Zie ook tabellen) |

| Na+ | Cl- | Na+ | Cl- | Na+ |
| Cl- | Na+ | Cl- | Na+ | Cl- |
| Na+ | Cl- | Na+ | Cl- | Na+ |
| Cl- | Na+ | Cl- | Na+ | Cl- |
| Na+ | Cl- | Na+ | Cl- | Na+ |
| Cl- | Na+ | Cl- | Na+ | Cl- |
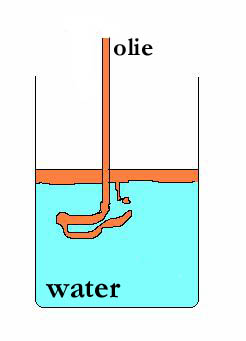
| keukenzout(aq) | |
| gedestilleerd water | |
| kalk(s) | |
| koper(s) | |
| leidingwater | |
| kalkwater | |
| kwik |
| Het is de bedoeling dat je een aantal stoffen gaat onderzoeken aan de hand van onderstaande 6 punten. | Je krijgt een potje met een nummer; je weet niet wat er in zit.
Na elke waarneming moet je proberen een (voorlopige) conclusie te trekken. |
| De te onderzoeken stoffen kunnen zijn: | De 6 aandachtspunten voor elke stof zijn: |
|
|