|
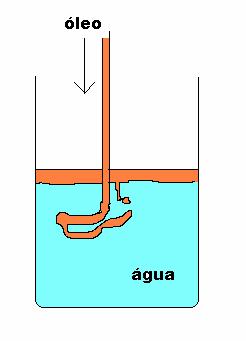
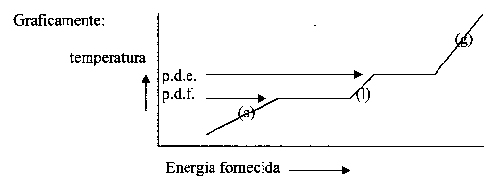
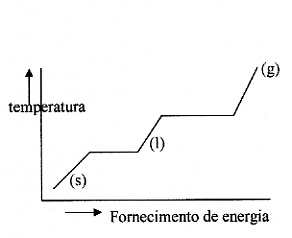
2. Substâncias puras & misturas 2.1 As fases; (s) (l) (g) (e aq) |
| partícula | Massa (g) | Massa (u.m.a) | Carga |
| Electrão | 9,1*10-28 | 0 | -1 |
| Neutrão | 1,67495*10-24 | 1 | 0 |
| Protão | 1,67254*10-24 | 1 | +1 |
|
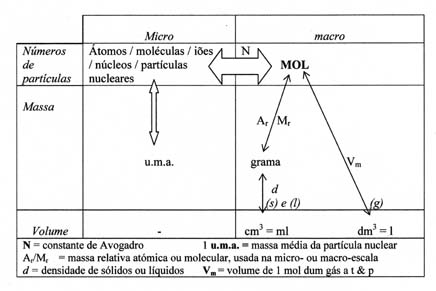
A unidade de qualquer massa do átomo = u.m.a.
Uma unidade de massa atómica podemos considerar a massa média de um nucleão. |
|
Um elemento pode ter diversos isótopos com números de massa diferentes.
A massa média dos isótopos, que normalmente se encontra nas tabelas na literatura, chamamos a massa atómica |
![]() 1 grama = 1/249,6 MOL
1 grama = 1/249,6 MOL
![]() 4 gramas = 4 x 1/249,6 MOL = 0,016 MOL
4 gramas = 4 x 1/249,6 MOL = 0,016 MOL
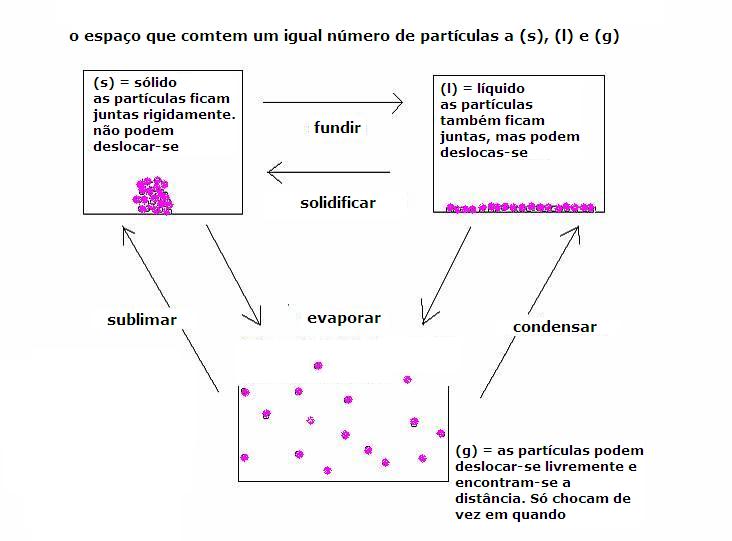
(s) |
(l) |
(g) |
|
(s) |
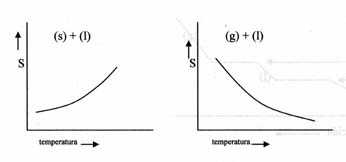
(s) + (s) | (s) + (l) | (s) + (g) |
(l) |
(l) + (s) | (l) + (l) | (l) + (g) |
(g) |
(g) + (s) | (g) + (l) | (g) + (g) |

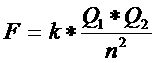

|
1. A REDE
Quais as forças dentro da rede do sólido? Fundir implica a destruição da rede e uma rede forte funda dificilmente. A força duma rede iónica depende em grande parte das cargas e dos raios iónicos. Uma rede de CaO (com cargas 2+ e 2-) vai fundir mais dificilmente do que a rede de NaCl (cargas 1+ e 1-). Iões pequenos (distância interiónica é menor) criam redes mais fortes. Normalmente, os sais têm pontos de fusão altos. As redes metálicas também dependem das cargas (quantos electrões livres, carga dos iões) e da distância entre as partículas. Existem grande diferenças entre os metais: Em geral, os metais têm redes fortes e, consequentemente, pontos de fusão altos. Alguns excepções são: Mercúrio (l), Chumbo, Estanho, Lítio, Sódio, Potássio não têm redes muito fortes. Extremamente fortes são as redes de Cromo, Wolfrámo e Vanádio (veja a tabela V) |
|
2. AS FORÇAS VANDERWAALS Nas redes molecularesexistem forças VanderWaals que dependem de:
|
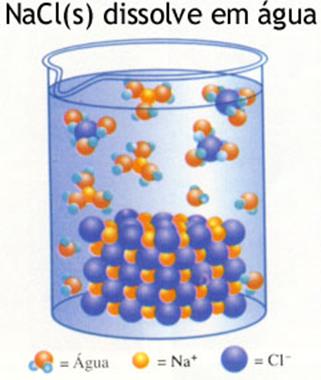
| Na+ | Cl- | Na+ | Cl- | Na+ |
| Cl- | Na+ | Cl- | Na+ | Cl- |
| Na+ | Cl- | Na+ | Cl- | Na+ |
| Cl- | Na+ | Cl- | Na+ | Cl- |
| Na+ | Cl- | Na+ | Cl- | Na+ |
| Cl- | Na+ | Cl- | Na+ | Cl- |