De structuur van een indikator is meestal organisch en behoorlijk complex.
Heel vaak gebruiken we een afgekorte formule: HIn.
Die H is natuurlijk het proton dat afgestaan kan worden (de indikator is een zwak zuur) en de rest - In - geeft het grootste en ingewikkelde deel van het molecuul aan.
In module 8 gebruikten we al een voorbeeld van een stof die de mogelijkheid heeft om de ligging van zijn evenwicht zichtbaar te maken. Dat was dus een indikator.
De zuur-base indikator functioneert dus omdat HIn een andere kleur heeft dan In-.
De indikatoren in tabel VIII zijn allemaal zuur-base indikatoren.
Er bestaan ook redox-indikatoren die we gebruiken bij redoxtitraties (andere module).
De zuur-base indikator is zelf meestal een organisch zwak zuur met een nogal complexe structuur. Afgekorte formule: HIn.
In water:
HIn + H2O
 H3O+ + In- (evenwicht IND)
H3O+ + In- (evenwicht IND)
HIn heeft kleur 1 In- heeft kleur 2
Stel je deze indikator voor in zuur milieu, bijvoorbeeld in een oplossing van zoutzuur.
In dat milieu domineren de (H3O+)-ionen en het evenwicht IND verplaatst zich naar links. Je kunt ook zeggen dat in zuur milieu de indikator vooral de vorm aanneemt van HIn, en dus overheerst de kleur 1.
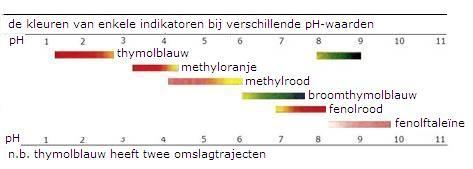
Elke indikator heeft een omslagtraject die je kunt vinden in de tabel.
Een voorbeeld: Methyloranje heeft een omslagtraject van 3,1 - 4,4 (rood-oranje)
Stel je een sterk aangezuurde oplossing voor met pH=1. Doe je er een paar druppels van het Methyloranje bij dan krijgt de oplossing de kleur rood.
Nu gaan we sterke base toevoegen (KOH(aq)) en het zuur wordt beetje bij beetje geneutraliseerd en de pH-waarde zal langzaamaan stijgen. Het begon met pH=1, langzaam stijgt die waarde.
Als de waarde 3,1 wordt gepasseerd dan begin je kleurverandering te zien van rood naar oranje. Pas bij het bereiken van de pH-waarde 4,4 is de kleur echt definitief oranje geworden.
Binnen de overgangszone, het omslagtraject, zal de kleur een mengvorm zijn van de twee kleuren.
In het omslagtraject van de indikator ligt het evenwicht niet erg links en niet erg rechts.
Nogmaals: de kleur van de indikator hangt af van het milieu van de oplossing.
In zuur milieu ligt evenwicht IND links en dan overheerst de kleur van de moleculen HIn.
Heb je gezien dat het omslagtraject lang niet altijd in de buurt van de 7 ligt?!