Verbranding, volledig en onvolledig
Ook in de koolstofchemie komen redoxreacties voor. Veel koolstofverbindingen zijn in staat om elektronen af te staan of op te nemen.
Let wel: als er hier over oxidatie wordt gesproken, dan wordt niet bedoeld de directe verbranding met zuurstof.
Haast alle stoffen uit de koolstofchemie zijn wel te verbranden tot koolzuurgas en waterdamp, maar daarover gaat het hier niet!
Wel geef ik even een kort een overzicht van directe en indirecte verbranding, maar daarna gaan we naar de bedoelde redoxreacties.
Volledige verbranding
Een mooi voorbeeld van volledige verbranding (maar toch in stappen) zie je in opdracht 39.
Hier krijg je alvast de reactie:
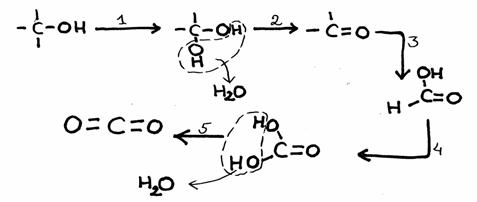
Vrijwel alle koolstofverbindingen (met C en H en andere elementen) reageren sterk met zuurstof.
Het meest reactieve element is dan waterstof dat meteen - in contact met zuurstof - water vormt.
Daarna (d.w.z. het gebeurt vrijwel gelijktijdig) reageert het koolstof en vormt CO2. Eventueel aanwezig S of N of P of ander elementen kunnen meer producten maken zoals SO2 en de stikstofoxides NxOy. Deze (gasvormige) producten zijn verantwoordelijk voor de luchtvervuiling.
Logisch dat de beste benzine zo weinig mogelijk zwavel en stikstof bevat.
Onvolledige verbranding
Dat vindt plaats als er onvoldoende zuurstof is.
H gaat als eerste natuurlijk weer over in water, maar om het koolstof te verbranden is dan niet genoeg zuurstof voorradig (er kan bijvoorbeeld niet genoeg lucht bij). Dan vormt zich CO (koolmonoxide) of zelfs kan het koolstof onverbrand blijven (roetvorming).
Zorg er voor dat je altijd de stoffen verbrandt bij voldoende luchttoevoer.
Koolmonoxide wordt ook wel kolendamp genoemd, dat herinnert aan de vroegere kolenkachels.
