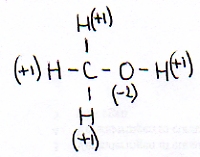
| Ethaan | Beide C-atomen zijn -3 |
| ethanol | één C-atoom is -3 en de ander is -1 |
| ethanal | één C-atoom is -3 en de ander is +1 |
| ethoxi-ethaan | Twee C-atomen zijn -3 en twee andere zijn -1 |
| ethylethan(o)aat | Twee C-atomen zijn -3, één is +1 en één is +3 |
| methaan | Het C-atoom is -4 |