monosachariden
Dit zijn de monomeren van de polysachariden. Er zijn diverse typen monosachariden, afhankelijk van:
- het aantal C-atomen: tetrose, pentose, hexose, heptose
- de aanwezigheid van een aldehyde- of ketongroep: aldose en ketose
- de structuur van het hele molecuul, lineair of open, dan wel cyclisch of gesloten
Vijf voorbeelden van monosachariden:
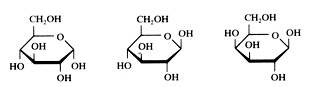
Glucose α en β en Galactose
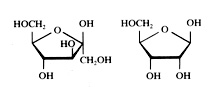
Fructose en Ribose
De monosacchariden kunnen zich bevinden in een lineaire of in een cyclische vorm (hierboven zie je alleen cyclische vormen).
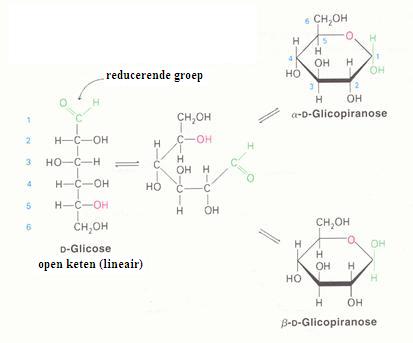
Je kunt in onderstaande schema zien hoe glucose de lineaire en de cyclische vorm kan aannemen:
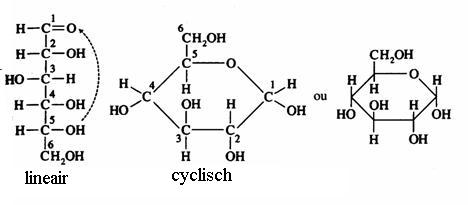


de cyclische structuur van glucose
De lineaire structuur kan gemakkelijk geoxideerd worden, dus met een zwakkere oxidator; vaak gebruikt men:
Ag+ ammoniakale zilveroplossing = reagens van Tollens. Ook Fehlings' reagens werkt prima (Cu2+)
De cyclische vorm wordt niet gemakkelijk geoxideerd (er is geen =O binding voorradig).
Het is in de praktijk nu eenmaal zo dat de twee structuren, de lineaire en de cyclische in oplossing met elkaar in evenwicht zijn, dus dat de lineaire structuur er altijd bij zit en die laat zich goed oxideren.
Omdat de lineaire tijdens dat proces verdwijnt en in evenwicht is met de cyclische, zal de cyclische vorm steeds meer overgaan in lineaire vorm, oftewel, alles wordt uiteindelijk toch geoxideerd.
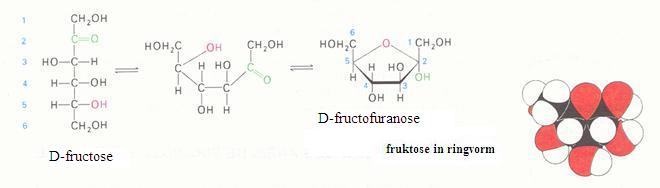
Bestudeer goed de volgende twee afbeeldingen: glucose en fructose komen op twee manieren voor, de lineaire en de ciclische. De twee vormen zijn - in waterig milieu, altijd in evenwicht met elkaar.
Toch heeft alleen de lineaire structuur de juiste groep om te oxideren (de reductorgroep).
Tijdens het redox-proces verdwijnt toch niet alleen de lineaire vorm, maar ook de ciclische vorm.