Het meest beroemde voorbeeld is het aluminium-ion in water opgelost, maar er zijn er veel meer. Kationen zijn vrijwel altijd meerwaardige gehydrateerde positieve metaalionen: Al(H2O)63+, Cu2+, Fe2+ of Fe3+, en nog veel meer andere, zijn altijd in water gehydrateerd.
hydratatie
De positieve ionen trekken, in watermilieu, de negatieve kanten van de watermoleculen aan, om zich heen.Vervolgens veroorzaken ze een afstotende werking tussen het centrale positieve ion en de δ+)ladingen van de H-atomen van de watermoleculen. Er is dan een neiging om H+ af te stoten.
Een oplossing van, bijvoorbeeld IJzer(III)chloride kan op die manier een behoorlijk zure pH verkrijgen.
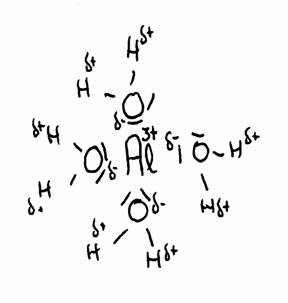
De tekening laat de aantrekking zien tussen Al3+ en het δ- deel van zuurstof en het δ+ deel van waterstof.
De watermoleculen (in totaal 6) omgeven het 3+ ion van Aluminium omdat dit positieve ion de δ- van water om zich heen trekt.
Zodoende wordt de afstand tussen 3+ en δ+ steeds korter en daarmee de afstoting tussen 3+ en δ+ steeds sterker.
Het gevolg is dat de H min of meer kan worden afgestoten. Er kan afgifte zijn van H+-ionen, en dat noem je: een zuur karakter. (zie veel meer hierover in module 9)
Opdracht 9
Leg het zure karakter uit van het ammonium-ion, door alleen maar een reactievergelijking op te schrijven.
Kies antwoord 04-09
terug naar start