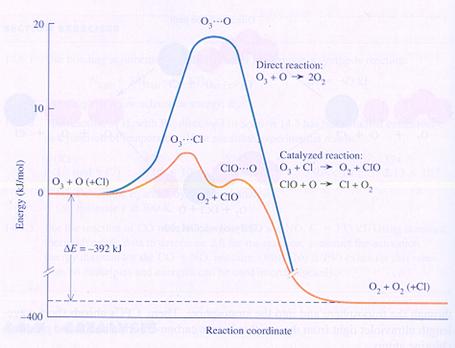
Energiediagram, Exotherm, Endotherm
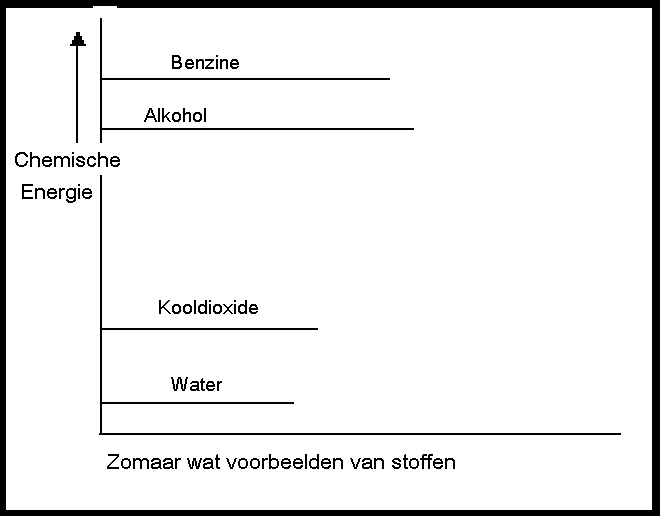
Als benzine reageert met zuurstof (dat zijn twee behoorlijk energierijke stoffen) vormen zich de producten water en koolzuurgas (twee stoffen met heel weinig interne energie).
Het systeem verliest dus een boel chemische energie tijdens deze verbranding. Die verdwijnt niet zomaar, want energie gaat niet verloren. Die komt naar buiten; in dit geval in de vorm van warmte.
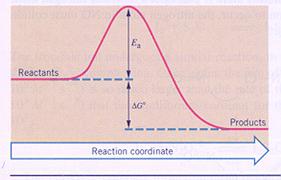
ΔGo geeft de reactie-energie aan waarvoor men vaak ook het symbool ΔH gebruikt.
Eais de activerings-energie.
Als er energie wordt opgenomen door een systeem, krijgt ∆H een positieve waarde. Het systeem wint energie. We spreken van een 'endotherme' reactie.
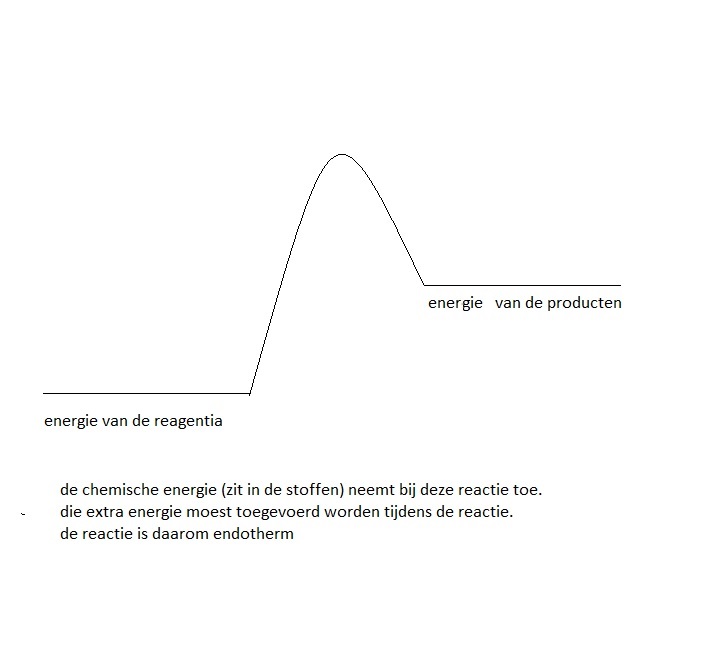
Als er energie wordt afgegeven door een systeem, krijgt ∆H een negatieve waarde. Het systeem verliest energie. We spreken van een 'exotherme' reactie.
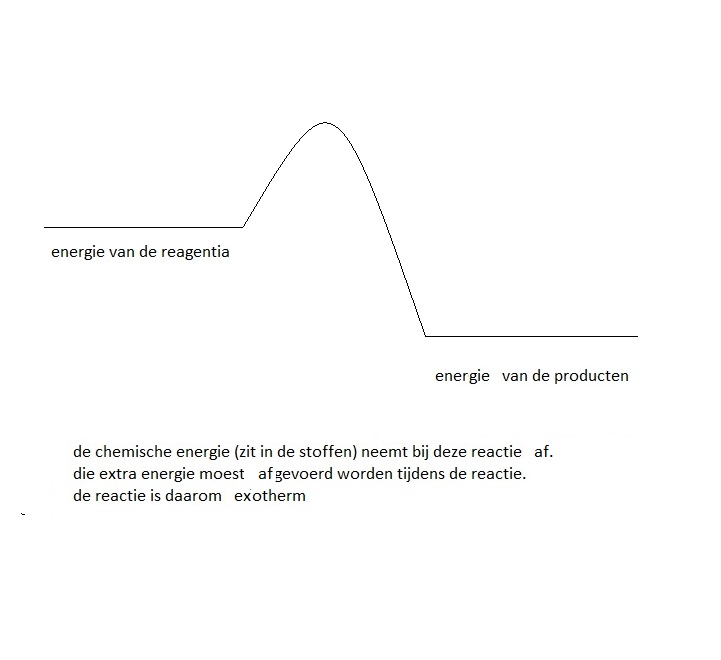
een diagram waarin verschillende stappen van de reactie zichtbaar worden: