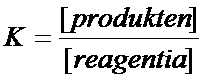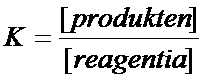De evenwichtsconstante bevat de concentraties van die stoffen die homogeen aanwezig zijn. In dit geval voeg je een C toe aan de K: KC .
Een andere homogene situatie is het geval van een gas-evenwicht. Dan spreken we niet zozeer van concentraties, maar wel van de (partiële) gasdruk van elk deelnemend gas. Elk gas in een gasmengsel draagt bij aan de druk.
De partiële druk van elke komponent is evenredig met de hoeveelheid van dat gas.
In de formule van de evenwichtsconstante vullen we hier de waarden in van die partiële drukken; de formule verandert niet in werkelijkheid, maar de K wordt soms aangegeven met KP.
resumerend:
- In homogene oplossingen gebruiken we KC
- Bij gassen gebruiken we KP
- Bij heterogene mengsels (s)+(aq) in evenwicht gebruiken we Ks
- Volgens afspraak wordt de "concentratie" van een vaste, heterogene stof de waarde 1 gegeven.
- De waarde van K hangt niet af van veranderingen in concentraties, druk of katalysator,
Die verandert alleen als de temperatuur van het systeem in evenwicht verandert.
Er zijn veel evenwichten met extreem sterke stoffen aan één kant en heel zwakke stoffen aan de andere kant van de pijlen.
Nogmaals: als evenwicht bereikt is kunnen de concentraties aan beide kanten zeer verschillend zijn. Vrijwel zeker zal er heel veel zijn van de zwakke en heel weinig van de sterke stoffen.
Zo'n evenwicht ligt sterk aan één kant.
Dat zie je meteen aan de formule voor K en de waarde van K:
Opdracht 17
Welke waarde heeft K:
- als er zeer sterke producten en zeer zwakke reagentia meedoen
- als er zeer zwakke producten en zeer sterke reagentia meedoen
Kies antwoord 08-17
terug naar start